
Une nouvelle classe de molécules contre les cellules cancéreuses réfractaires aux traitements conventionnels
|
Une nouvelle classe de molécules capables d’induire la mort des cellules cancéreuses réfractaires aux traitements standards et responsables des récidives a été conçue par des scientifiques de l’Institut Curie, du CNRS et de l’Inserm. Cette avancée cruciale dans la lutte contre les cancers métastatiques tire son origine de l’identification du site cellulaire d’initiation de la ferroptose, un processus naturel qui provoque la dégradation oxydante des membranes des cellules, catalysée par le fer. Ces résultats précliniques prometteurs sont publiés dans la revue Nature le 07 mai 2025.
Les traitements anticancéreux actuels ciblent essentiellement les cellules tumorales primaires qui prolifèrent rapidement, mais ne permettent pas d’éliminer efficacement les cellules cancéreuses à potentiel métastatique1 , capables de s’adapter aux traitements existants. Or les métastases sont responsables de 70 % des décès par cancer.
Une équipe de recherche française pilotée par des scientifiques de l’Institut Curie, du CNRS et de l’Inserm vient de mettre au point une nouvelle classe de petites molécules capables de provoquer la destruction des membranes cellulaires et donc la mort des cellules. Menée par des scientifiques du Laboratoire de Biomédecine (Institut Curie/CNRS/Inserm)2 , cette étude s’appuie sur les propriétés remarquables des cellules cancéreuses dites persistantes, à fort potentiel métastatique ; elles expriment à leur surface une grande quantité d’une protéine appelée CD44 qui leur permet d’internaliser du fer ce qui leur confère une plus grande agressivité et une capacité accrue à s’adapter aux traitements conventionnels. Ces cellules sont ainsi plus sensibles à la ferroptose, un processus de mort cellulaire catalysée par le fer qui engendre l’oxydation et la dégradation des lipides membranaires.
Grâce à une chimie innovante développée par l’équipe dirigée par Raphaël Rodriguez, les chercheurs ont montré que la mort cellulaire initiée par le fer dans les lysosomes3 peut conduire à une altération de l’organisation des compartiments membranaires intracellulaires. Dans le compartiment lysosomal, le fer réagit avec du peroxyde d’hydrogène, générant des radicaux oxygénés, entités chimiques très réactives qui endommagent les membranes cellulaires. Cette réaction en cascade se propage ensuite dans la cellule, formant des lipides peroxydés dans les membranes d’autres organites cellulaires, causant in fine la mort de la cellule. La ferroptose est ainsi le résultat d’un échec de la cellule à réparer les dommages des membranes.
Forts de leurs premières découvertes, ces scientifiques ont réussi à concevoir et synthétiser une nouvelle classe de petites molécules capables d’activer la ferroptose : les dégradeurs de phospholipides. Celle-ci disposent d’un fragment permettant de cibler la membrane cellulaire (membrane plasmique) et ensuite de s’accumuler dans les lysosomes par endocytose, et d’un autre fragment capable d’exacerber la réactivité du fer abondant dans ce compartiment des cellules cancéreuses pro-métastatiques, ce qui va déclencher la ferroptose. Une molécule, la fentomycine (Fento-1), a été conçue de manière à être fluorescente, permettant aux scientifiques de la visualiser dans la cellule par microscopie de fluorescence et de confirmer sa localisation dans les lysosomes.
Après administration de Fento-1, les chercheurs ont observé une réduction significative de la croissance tumorale dans des modèles précliniques de cancers du sein métastatiques ainsi qu’un effet cytotoxique prononcé sur des biopsies de cancers du pancréas et de sarcomes de patients, confirmant l’efficacité du traitement au niveau pré-clinique4 sur ces cancers pour lesquels l’efficacité des chimiothérapies conventionnelles est limitée.
Des études cliniques sont nécessaires pour démontrer que cette capacité d’induire la ferroptose pourra être une voie thérapeutique complémentaire aux chimiothérapies actuelles dans la lutte contre les cancers en ciblant particulièrement les cellules cancéreuses pro-métastatiques et réfractaires aux traitements conventionnels.
Ces travaux ont notamment bénéficié du soutien de la Ligue contre le cancer (3 Equipes Labellisées), du programme de la recherche et de l’innovation Horizon 2020 de l’Union Européenne ERC, de la Fondation pour la recherche médicale, de la Fondation Charles Defforey–Institut de France, de la Fondation Klaus Grohe, de l’Institut national du cancer, de la région Ile-de-France, de l’ANR, de la Fondation Bettencourt Schueller, du CNRS, de l’Institut Curie et de l’Inserm.
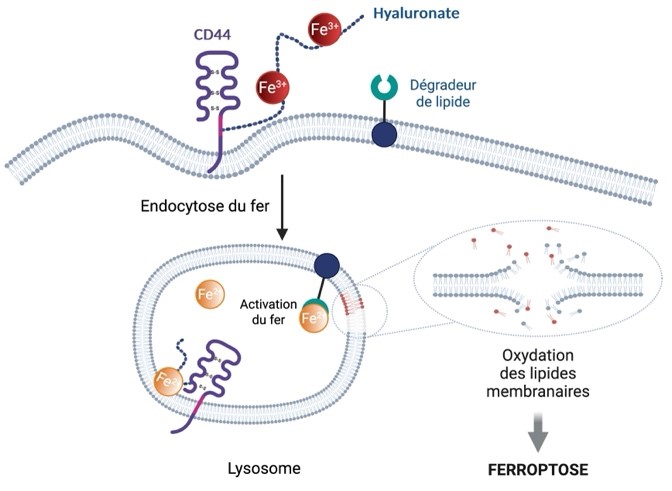
Schéma de la ferroptose. Le fer pénètre dans les cellules cancéreuses via la protéine CD44 présente à leur surface lui permettant d’acquérir des propriétés métastatiques et de tolérance aux traitements conventionnels par reprogrammation épigénétique qui joue un rôle clé dans l’adaptation cellulaire. L’activation du fer lysosomal par un dégradeur de phospholipides provoque l’oxydation et la rupture des membranes cellulaires, entraînant ainsi la mort de la cellule.
- 1Cellules tumorales qui se détachent de leur site d'origine pour migrer vers d'autres parties du corps, formant de nouvelles tumeurs appelées métastases. Cette capacité à se propager est une caractéristique des cancers avancés.
- 2Ces travaux impliquent principalement des scientifiques du Laboratoire de Biomédecine (Institut Curie/CNRS/Inserm/PSL Research University), du Centre de recherche en cancérologie de Marseille (Aix-Marseille Université/CNRS/Inserm/Institut Paoli Calmette), de l’APHP (Hôpital Paul-Brousse) et de l’Institut de chimie moléculaire et des matériaux d’Orsay (CNRS/Université Paris-Saclay).
- 3Les lysosomes sont des organites responsables de la dégradation des débris cellulaires, des macromolécules biologiques, des particules étrangères (bactéries, virus et parasites) et des organites intracellulaires endommagés.
- 4Les tests pré-cliniques chez l’animal ont montré une réduction significative du volume des tumeurs après injection lymphatique de Fento-1, avec une excellente tolérance au traitement.
Activation of lysosomal iron triggers ferroptosis in cancer


